
|

|

|

|

|

Insuficiencia Renal Aguda
Definición
La Insuficiencia Renal Aguda se caracteriza por la FALLA SÚBITA DE LA FUNCIÓN RENAL (FILTRACIÓN GLOMERULAR), usualmente en respuesta a una severa enfermedad aguda en algún sistema del organismo humano o en los riñones mismos. Otra característica es que es generalmente reversible cuando la condición subyacente es resuelta.Característicamente se observa un aumento de urea, creatinina en la sangre, sin embargo inicialmente solo se podrá observar disminución del volumen urinario. Un aumento de 0.5 mg% de creatinina en 24 horas y un volumen urinario diario menor de 400 cc al día, determinar la presencia de esta entidad.
Un aumento solo de Urea puede observarse con casos de sangrado digestivo, uso de esteroides, sobrecarga proteica en la alimentación, etc.
Basados en la cantidad de orina eliminada en un periodo de 24 horas, los pacientes pueden ser clasificados en:
- Insuficiencia Renal Aguda OLIGURICA: Excretan menos de 400 cc en 24 horas.
- Insuficiencia Renal Aguda NO OLIGURICA: Excretan más de 400 cc en 24 horas. Usualmente tiene un pronóstico más favorable.
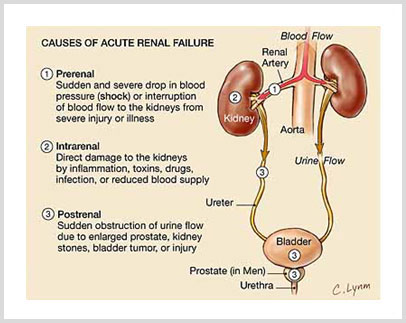
Causas de la Insuficiencia Renal Aguda
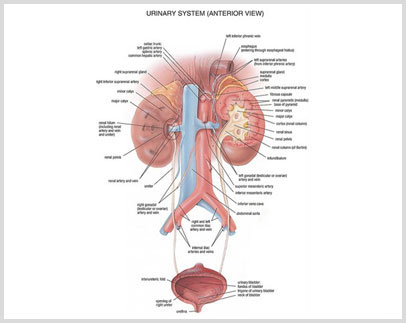
PRE RENAL
- Hemorragia Interna o Externa
- Insuficiencia de algún órgano: Cardiaca, Hepática, Pulmonar
- Shock anafiláctico
- Shock Séptic
- Deshidratación severa: Diarrea, fiebre, diuréticos, vómitos, etc
RENAL
- Progresión de los casos mencionados en 1
- Glomérulo nefritis
- Nefrotoxicidad por drogas: Anti inflamatorios, Amino glucósidos, Radio contraste
- Nefrotoxicidad por pigmentos: Hemólisis, Rabdomiolisis
- Enfermedad Vascular: Trombos, émbolos, vasculiti
- Rechazo de Injerto trasplantado
POST RENAL
- Cálculos Renales o de vías urinarias
- Tumores en vías urinarias
- Tumores en sistema ginecológico
- Estrechez de la Vía Urinaria
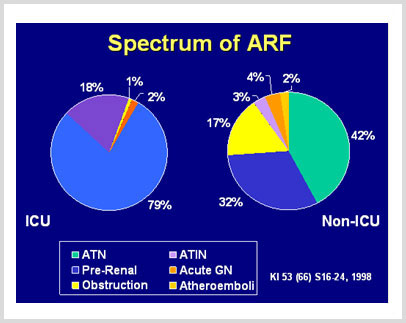
Epidemiología
La Insuficiencia Renal Aguda ocurre aproximadamente en el 1 % de las hospitalizaciones y ocurre ENTRE 2 Y 5 % DURANTE LA ESTANCIA HOSPITALARIA.De los pacientes que desarrollan Insuficiencia Renal Aguda durante la estancia hospitalaria, el 60 % de casos se presentan en pacientes quirúrgicos o traumatológicos, mientras el 40% son pacientes con padecimientos clínicos o con patología obstetrica.
De todos estos, se estima que EL 50% SON DE ORIGEN IATROGÉNICO Y POR LO TANTO POTENCIALMENTE EVITABLES.
Los nefrólogos son interconsultados en aproximadamente 70 casos por millón de habitantes.
El 0.5 % de los pacientes hospitalizados requieren de soporte dialítico. Sin embargo en pacientes que ingresan a una Unidad de Cuidados Intensivos, la incidencia varia entre un 7 a 30%, siendo las causas de índole renal parénquima las mas frecuentes.
Pronostico
Los pacientes con mayor riesgo de desarrollar Insuficiencia Renal Aguda son:- Hipertensión Arterial
- Diabetes Mellitus
- nsuficiencia Cardiaca Congestiva
- Mieloma Múltiple
- Infección Crónica
- Personas de la tercera edad. (mayor de 60 años)
Síntomas de la Insuficiencia Renal Aguda
- Falta de apetito (Anorexia)
- Fatiga
- Palidez
- Cambios en el estado mental
- Picazón en el cuerpo (prurito)
- Convulsiones
- Tremor en las manos
- Dificultad para respirar (diseña)
- Hinchazón del cuerpo (edema)
- Hipotensión arterial
Complicaciones de la Insuficiencia Renal Aguda
- Edema generalizado
- Uremia
- Hiperkalemia
- Pericarditis
- Neumonitis
- Encefalopatía
- Hemorragia gastrointestinal
- Acidosis Metabólica
- Alteraciones electrolíticas: Hiponatremia, Hipocalcemia, Hipermagnesemia, etc.
- Arritmia cardiaca
- Edema pulmonar
Exámenes Auxiliares
- Hemograma
- Hemoglobina
- Urea
- Creatinina
- Electrolitos
- Calcio
- Ácido Úrico
- Fósforo
- Gases Arteriales
- Glucosa
- Perfil completo Hepático
- Perfil completo de coagulación
- Lamina periférica
- Perfil Inmunoserologico
- Examen completo de orina
- Electrolitos urinarios
- Proteinuria de 24 horas
- Ecografía Renal y de vías urinarias
- Ecodoppler Renal
- Radiografía de Tórax
- Eco cardiografía, Electrocardiografía
- Gama grafía Renal
- Biopsia Renal
Tratamiento
- LO PRIMORDIAL ES EL TRATAMIENTO DE LA CONDICIÓN CLÍNICA DE FONDO.
- La detección temprana y el tratamiento precoz y agresivo de las entidades clínicas de fondo serán pilares fundamentales
- Mantener adecuado estado de Hidratación
- Uso de vasopresores de ser necesario
- Fenoldopam
- Péptidos Natri uréticos
- Antagonistas de receptores de Endotelina
- Evitar medicamentos Nefrotoxicos
- Diuréticos
- Infusión de Bicarbonato
- Manejo de la Hiperkalemia
- Diálisis: Hemodiálisis
- Hemofiltracion
- Nutrición
Insuficiencia Renal Crónica
Definición
La Insuficiencia Renal Crónica es una entidad clínica en la cual los riñones (ambos) son incapaces de cumplir con la función de filtración glomerular.Cuando este deterioro tiene una duración mayor de 3 meses, usualmente es irreversible, de curso es lento y los síntomas importantes se presentan tardíamente.
Funciones del Riñón
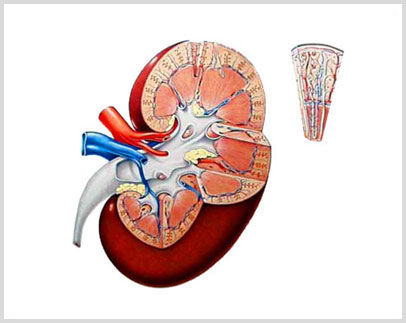
- Limpian el cuerpo de impurezas y eliminan los componentes químicos que están de más en la sangre y que el organismo no necesita, esto lo hacen a través de la orina. (FILTRACIÓN GLOMERULAR)
- Eliminan el líquido extra y regulan el una serie de electrolitos en nuestro cuerpo, el equilibrio Hidroeleectrolitico. (FUNCIÓN TUBULAR)
- Ayudan a mantener la presión de la sangre dentro de los límites normales. (Función Hormonal: RENINA)
- Protegen los dientes y los huesos, evitando que pierdan minerales como calcio, que los mantiene fuertes y duros. (Función Hormonal: VITAMINA D3, PARATOHORMONA)
- Ayudan a regular la producción de los glóbulos rojos, manteniendo un nivel normal de Hemoglobina. (Función Hormonal: ERITROPOYETINA)
Causas más frecuentes de la Insuficiencia Renal Crónica
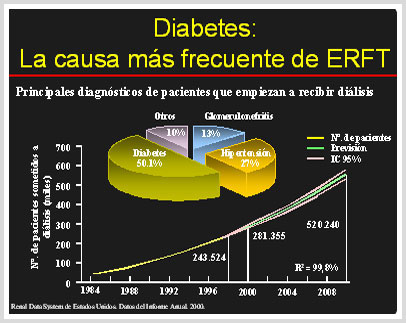
- DIABETES MELLITUS (60 – 50 % DE LOS CASOS)
- HIPERTENSIÓN ARTERIAL ( 20 – 30 % DE LOS CASOS)
- Procesos inflamatorios renales, denominados Glomerulonefritis, usualmente de origen auto inmune. (10 – 40 %)
- Pielonefritis Crónica
- Lupus Eritematoso Sistémico
- Enfermedad Vascular: Ateroesclerosis sistémica, Ateromas, etc.
- Trastornos Hereditarios (2- 8 % de los casos, usualmente en niños)
- Problemas congénitos del riñón (Enfermedad Renal Poliquistica 2 – 8 % de los casos) y de las vías urinarias (Reflujo Vesico Ureteral 10 – 20 % de los casos, usualmente en niños).
- Enfermedad Renal debido a tóxicos. (Nefrotoxicidad)
- Problemas obstructivos por tumores o cálculos (Litiasis Renal – 7 – 10 % de los casos)
- Causa desconocida
Causas más frecuentes de la Insuficiencia Renal Crónica
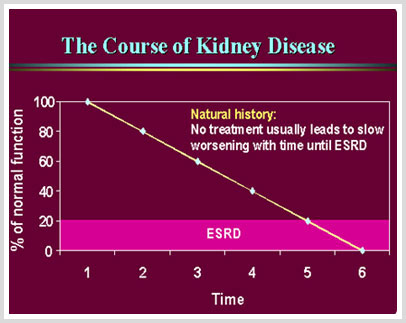
- USUALMENTE EL CURSO ES INDOLENTE Y SIN SÍNTOMAS
- Orinar constantemente durante la noche (Nocturia)
- Debilidad General
- Dolor de cabeza (Cefalea)
- Mareos
- Irritabilidad
- Perdida del apetito (Hiporexia – Anorexia)
- Picazón en el cuerpo (Prurito)
- Fatiga (Disnea)
- Calambres
- Piel pálida y terrosa, seca
- Hinchazón de pies y del cuerpo (Edema)
- Aumento de la presión arterial (Hipertensión Arterial)
- Aliento con olor a orina (Aliento Uremico)
- Dificultad para conciliar el sueño en la noche(Insomnio)
- Aumento del sueño en el día (Somnolencia)
- Falla en el crecimiento (en niños)
Grados de la Insuficiencia Renal Crónica – Enfermedad Renal Crónica
- Grado O - Pacientes con factores de riesgo para enfermedad renal crónica: Diabetes, Hipertensión, Lupus eritema toso, Litiasis renal, etc.
- Grado I - Filtración Glomerular mayor de 90 cc /min.
- Grado II - Filtración Glomerular de 60 a 89 cc /min.
- Grado III - Filtración Glomerular de 30 a 59 cc /min.
- Grado IV - Filtración Glomerular de 15 a 29 cc/min.
- Grado V - Filtración Glomerular menor de 15 cc/min.
- Filtración glomerular mayor de 90 cc/min.
- Evidencia de daño renal: Proteinuria, Hematuria, etc.
-Requiere iniciar Terapias de Reemplazo Renal
La Prevalencia de Enfermedad Renal Crónica es muy alta, en países donde se han realizado estudios en ese sentido han determinado altas tasas de prevalencia, cerca de 10 % de la población general padecería de algún grado de Enfermedad renal Crónica. El cuadro muestra los hallazgos en la población americana.
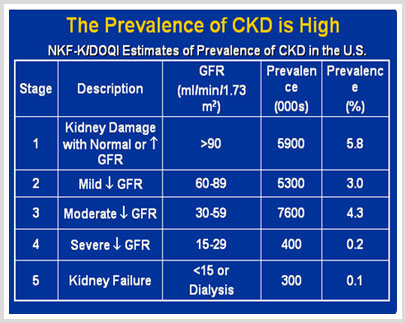
Complicaciones de la Insuficiencia Renal Crónica
- Desnutrición
- Anemia
- Osteodistrofia Renal
- Hipertensión Arterial
- Cardiopatía
- Edema Generalizado
- Riesgo de adquirir enfermedades víricas: Hepatitis Viral
- Gastritis
- Falla en el crecimiento (niños)
Exámenes Auxiliares
- DEPURACIÓN DE CREATININA DE 24 HORAS
- Urea
- Hemoglobina
- Calcio
- Fósforo
- Ácido Úrico
- Electrolitos Sericos
- Gases Arteriales
- Examen completo de orina
- Paratohormona
- Vitamina D3
- Albúmina serica
- Proteinuria de 24 horas
- Ecografía Renal y de vías Urinarias
- Gama grafía Renal Funcional
- Tomografía Renal
- Angio Tomografía Espiral Multicorte
Tratamiento
- Dieta Renal - EVITAR LAS CARNES ROJAS
- Ácido Fólico
- Complejo B
- Carbonato de calcio
- Vitamina D3
- Hormona de Crecimiento (niños)
- Tratamiento antihipertensivo: IECAs y/o BRATs
- Eritropoyetina
- Vacunación contra Hepatitis B
- Diálisis
- Trasplante Renal
- Evitar Gaseosas
- Evitar la sal
- Evitar alimentos con alto contenido de potasio (en estadios avanzados): Palta, chocolates, frijoles, cítricos, melón, hongos, berros, espinacas, repollo, jugos enlatados, plátanos.
- El volumen de liquido estará de acuerdo al volumen de orina en el día - Condimente los alimentos con especies naturales
Hemodiálisis Crónica Ambulatoria
Los RIÑONES tienen la función de limpiar la sangre de las sustancias tóxicas (UREA, CREATININA, FOSFORO, etc.) y de los líquidos que le sobran, que se eliminan en forma de orina, además de producir una variedad de hormonas y vitaminas (ERITROPOYETINA, RENINA, VITAMINA D3, etc.) necesarias para el organismo. Cuando en un paciente, por un problema de insuficiencia renal aguda, crónica o crónica reagudizada, los riñones dejan de funcionar (menos de 15 cc/min), la diálisis permite realizar mediante equipos médicos, las funciones de los riñones.
Existen básicamente dos tipos de diálisis: Hemodiálisis y Diálisis Peritoneal.
La Hemodiálisis es un proceso terapéutico mediante el cual se elimina básicamente los desechos de la sangre. Asimismo se elimina el exceso de agua que se ha acumulado en el cuerpo del paciente.
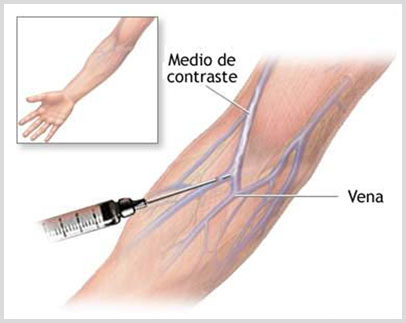
Para "limpiar" la sangre ante todo hace falta poder acceder a ella. Para ello se utilizan dos medios, bien un acceso al sistema venoso periférico denominado FISTULA o bien un acceso al sistema venoso central mediante algún tipo de CATETER artificial. En ambos casos se deben construir estos accesos pasando por una intervención quirúrgica.
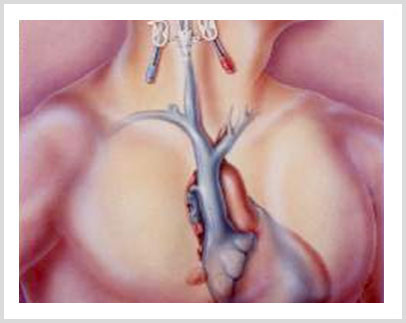
La FISTULA ARTERIO VENOSA es uno de los sistemas de acceso a la sangre para realizar la hemodiálisis. Lo que se hace quirúrgicamente es unir una arteria y una vena del brazo (usualmente en el brazo no dominante) para aumentar el volumen sanguíneo de la misma, requisito imprescindible para esta técnica. Este acceso es el método mas seguro, que dura más tiempo y tiene menos complicaciones (trombosis, infeccion, etc).
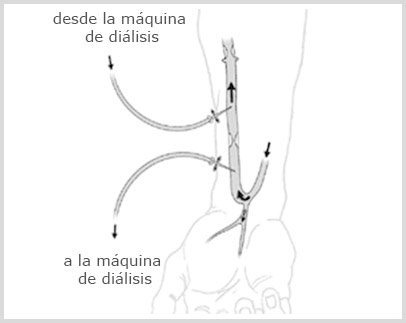
Para el tratamiento de hemodiálisis se insertan dos agujas en una vena previamente arteriolizada mediante una fístula, de esta manera ya tenemos el acceso venoso, y la SANGRE es extraída por una bomba mecánica de la MAQUINA DE HEMODIALISIS y a través de un sistema de tubos y de un FILTRO DIALIZADOR especial. Así se produce el intercambio entre el liquido del dializador (DIALIZADO) recogiendo las sustancias toxicas y limpiando así la sangre para luego ser devuelta al cuerpo. En el mismo procedimiento se aporta otras sustancias beneficiosas (Calcio, Bicarbonato, etc.).
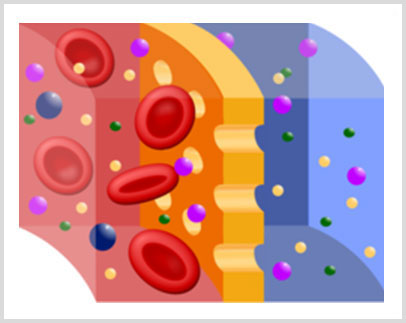
Durante una sesión de hemodiálisis, toda la sangre del cuerpo pasa varias veces a través del filtro o dializador. La mayoría de las personas necesitan dializarse TRES VECES POR SEMANA. La mayor parte de los enfermos reciben tratamientos en el ciclo de lunes-miércoles-viernes o martes-jueves-sábado. La mayoría de las sesiones de hemodiálisis duran entre 3 y 4 horas.
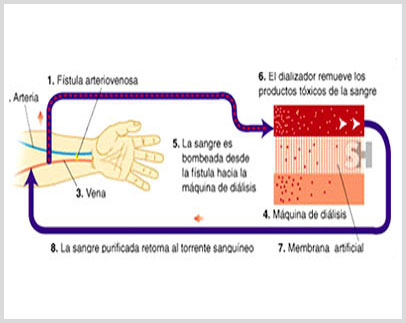
A semejanza de los riñones sanos, la diálisis permite:
- Eliminar las sustancias toxicas, la sal y el agua en exceso del organismo.
- Mantener el nivel adecuado de ciertas sustancias químicas en la sangre.
- Contribuye a controlar la Presión Sanguínea.
¿Que molestias puede presentar en la Hemodiálisis?
Cuando se inicia el tratamiento, es posible que la colocación de las agujas en la fístula, les resulten molestas y dolorosas, sin embargo la mayoría de los pacientes se acostumbran a ello con el tiempo. Existen cremas analgésicas que se pueden aplicar antes de la canulación.
Otras molestias son los calambres, dolores de cabeza, nauseas, vómitos o mareos, síntomas que pueden indicar la necesidad de corregir el peso seco, la concentración de sodio o la temperatura del liquido dializador, adecuar los tratamientos con medicamentes antihipertensivos que usa, o adoptar medidas en la ingesta calórico.
¿Que cuidados debe tener con la Fístula Arteriovenosa?
No olvide LAVARSE EL BRAZO donde esta la fístula con jabón desinfectante antes de ingresar a la Unidad de Diálisis. El centro le proveerá los insumos adecuados en el baño de pacientes
El control mediante la palpación del funcionamiento de la Fístula, notando una sensación de vibración al palparla con los dedos.
Protegiendo el brazo de golpes y rozaduras. Evitar coger mucho peso con el brazo de la fístula o comprimirlo con bolsos, relojes o pulseras.
No deberá extraerse sangre, ni tomarse la presión arterial en el brazo donde esta la Fístula.
Realizar los ejercicios con la mano o el brazo que el nefrólogo le indique, con el objetivo que mejore la circulación sanguínea en la Fístula.
¿Que vacunas debe tener el paciente en Diálisis?
- Anti Hepatitis B (Euvax – Engerix)
- Anti Tetanica
- Anti Neumococica (Pneumo 23)
- Anti Gripal (Influenza)
¿Que medidas debe adoptar antes y después de la Diálisis?
El paciente y sus familiares, deben PLANIFICAR Y ORGANIZAR las tareas diarias y el trabajo de acuerdo al calendario de sesiones. Esta recomendación tiene mayor relevancia cuando se debe viajar.
La PUNTUALIDAD al acudir a las terapia de Hemodiálisis es cardinal, en especial por el respeto a los demás pacientes que vienen al centro de Diálisis en los siguientes turnos.
Es importante la dedicación necesaria al CUIDADO PERSONAL y a la ALIMENTACION, de esta manera los inconvenientes se evitaran.
Acuda al centro con algún FAMILIAR, en especial si el paciente es mayor de edad o menor de edad. Asimismo si tiene alguna discapacidad.
Siempre lleve ROPA COMODA.
Después de la Diálisis, se recomienda estar un tiempo prudencial en REPOSO (aproximadamente 20 minutos) ya que es común la sensación de cansancio después del procedimiento.
En la dieta, deben suprimirse los frutos secos, tomate y cacao (POTASIO), las frutas, legumbres y verduras podrán consumirse con la indicación individualizada para cada paciente brindada por el Medico Nefrólogo o Nutricionista Renal. Para evitar el aporte de sodio, los alimentos deben cocinarse SIN SAL.
Para mejorar el sabor de los alimentos, se puede utilizar, ajo, orégano, estragón, romero, albahaca, tomillo, vinagre,etc. Utilice aceite de oliva en la preparación de alimentos.
Debe eliminarse el alcohol, el tabaco y drogas. Debe evitar Antiinflamatorios y toda medicación debe ser aprobada previamente por su Nefrólogo.
¿Donde se realiza el tratamiento de Hemodiálisis?
La Hemodiálisis se realiza en un centro sanitario, un CENTRO DE DIALISIS o en el propio domicilio.
El Servicio de Hemodiálisis Crónica Ambulatoria se brinda en el Centro de Hemodiálisis DIALYSIS SERVICE S.R.L., ubicado estratégicamente en el Distrito de Jesús Maria.

Hemodiálisis a Domicilio
Definición
La Hemodiálisis a Domicilio consiste en realizar el procedimiento en la casa del paciente, idealmente en un ambiente especial al interior del hogar.
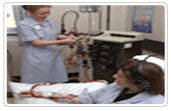
Al igual que en la Hemodiálisis Crónica Ambulatoria realizada en un Centro de Diálisis, se requiere de una serie de maquinas e insumos de diálisis.
El paciente y su familiar o asistente personal recibirán entrenamiento en el uso de dichas maquinas y de los insumos, para la realización adecuada de los procedimientos de Hemodiálisis y de la responsabilidad de su tratamiento.
La Hemodiálisis realizada en casa, permite a los pacientes dializarse más frecuentemente y por un mayor periodo de tiempo que en los Centros de Diálisis.
Las diversas investigaciones has demostrado que se obtienen mejores resultados clínicos.
- Mejoría en la CALIDAD DE VIDA
- Mejora en la sensación de bienestar
- Incremento en la flexibilidad de la Dieta
- Mejor control de la Hipertensión Arterial
- Mejor patrón de sueño
- Menor sintomatología relacionada a la fatiga y las nauseas
- Necesidad reducida de medicamentos
- Disminución en la frecuencia de complicaciones en la fístula arteriovenosa.
- MENOR TASA DE HOSPITALIZACIONES.
- MAYOR TASA DE SOBREVIDA.

¿Qué requisitos se necesita para estar en tratamiento de Hemodiálisis a Domicilio?
- Capacidad de aprender todo lo relacionada a la Diálisis.
- Deben recibir entrenamiento en el Centro de Diálisis o Clínica, durante un periodo de 4 semana.
- Capacidad de adaptarse a las necesidades del equipamiento en casa.
- Adecuada destreza manual y adecuada visión para operar los equipos.
- Lectura y Escritura básica en relación a los manuales y documentos a redactar en cada diálisis.
- Adecuado espacio (con iluminación, modificaciones eléctricas, etc.) en el Hogar para la instalación de los equipos de diálisis.
- Mobiliario adecuado para la manipulación y almacenaje de los insumos.
- Mucha Iniciativa y Motivación.
- Asistente de Diálisis, quien podría ser una enfermera o técnico en diálisis, así como un familiar o amigo a quien se le capacitara previamente.
Evolución
El paciente acudirá mensualmente o cada 2 meses a sus controles médicos para los cuales deberá realizarse exámenes de laboratorio.
Algunas Novedades en Hemodiálisis Domiciliaria
Para incrementar la autonomía y la sensación de seguridad de los pacientes y de sus familiares, se debe considerar el uso de la TELE ASISTENCIA MEDIANTE TERMINALES MULTIMEDIA.
A través de estos sistemas, se transmiten mensajes de voz, datos e imágenes.
Mediante el teléfono móvil, el paciente establece comunicación una comunicación permanente con el Nefrólogo o Enfermera especializada, soluciona sus dudas puntuales y recibe recomendaciones del equipo médico, además de conectar las maquinas dializadoras entre el domicilio y el Centro de Diálisis, permitiendo así la monitorización a la distancia del paciente.
Realidad Actual
A pesar de las ventajas reconocidas de la Hemodiálisis domiciliaria así como de otras formas de Diálisis Domiciliaria, la aplicación de estas técnicas no alcanza a mas del 10% de los pacientes en Diálisis en la mayoría de los países donde esta terapia esta mas desarrollada.
El bajo porcentaje de Diálisis Domiciliaria es debido fundamentalmente a:
- Falta de Infraestructura en las Clínicas y Hospitales para la enseñanza programada.
- Temor del paciente y familiares a asumir el tratamiento en su domicilio y responsabilizarse de su auto cuidado.
- Costos
Otras formas de Diálisis Domiciliaria
- Hemodiálisis Domiciliaria Tradicional: Realizada 3 veces por semana, de 3 a 4 horas de duración.
- Hemodiálisis Domiciliaria Diaria: Realizada 5 a 6 veces por semana, de 2 horas 30 minutos de duración.
- Hemodiálisis Domiciliaria Nocturna: Realizada mientras el paciente duerme, 3 o mas noches a la semana.
- Diálisis Peritoneal Continua Ambulatoria: Realizada 4 a 5 veces por día, sin una maquina.
- Diálisis Peritoneal Automatizada: Realizada mientras el paciente duerme, en forma diaria y a través de una maquina electrónica automática denominada cicladora.


Hemodiafiltración
La difusión, convección y adsorción son los tres principios físicos que regulan la eliminación de sustancias en la diálisis extracorpórea. Los solutos de pequeño tamaño y gran movilidad se transfieren bien por difusión; en cambio, las moléculas medianas y grandes con poca movilidad se eliminan mejor por convección y adsorción.
Como la adsorción es difícil de cuantificar y de regular, para aumentar la transferencia de solutos hay que recurrir a procedimientos que potencien la difusión y la convección.
Las técnicas de diálisis utilizadas en el tratamiento sustitutivo de la insuficiencia renal crónica se clasifican en dos grandes grupos según predomine el principio de difusión (hemodiálisis) o de convección (hemofiltracion)
Las técnicas convectivas surgen con la finalidad de aumentar la eliminación de las moléculas de mediano y gran tamaño que se transfieren mal por difusión. La transferencia de solutos en la convección se realiza mediante el principio de arrastre por flujo y depende del tamaño del poro de la membrana y de la tasa de ultrafiltración. Las técnicas convectivas usan una membrana de gran permeabilidad y realizan una ultrafiltración superior a la necesaria para eliminar el líquido acumulado por el enfermo entre dos sesiones de diálisis. El exceso de volumen extraído debe ser repuesto con un líquido de sustitución de composición fisiológica.
Las técnicas convectivas pueden utilizar exclusivamente el principio de convección sin difusión (hemofiltración), o tratarse de técnicas mixtas que, sin abandonar el principio de difusión, utilizan diversas formas de convección (hemodiafiltración).
Los procedimientos convectivos pueden clasificarse, a su vez, en dos grupos según el líquido de reposición sea una solución de electrolitos contenidos en bolsas (convección clásica) o el propio baño de diálisis convenientemente tratado (convección online).
La hemodiafiltración veno–venosa continua (HdFVVC), es una de estas técnica de purificación sanguínea diseñadas para remover los productos metabólicos de desecho acumulados en la sangre a través de un mecanismo combinado de transporte difusión y de transporte convectivo a través de una membrana semipermeable de alto flujo que tiene un coeficiente de ultrafiltración mayor de 200 cc/hora/mmHG/mt2 y un coeficiente de sieving para B2 microglobulina de mas de 0.6. El volumen convectivo efectivo debe ser al menos del 20 % del total de volumen sanguíneo procesado. El líquido es removido por ultrafiltración y el volumen del líquido filtrado excedente de la perdida de volumen deseado es reemplazado por la infusión externa y continua de una solución libre de pirógenos y estéril hacia el torrente sanguíneo del paciente... La HDF provee una mejor eliminación de solutos de alto peso molecular que la hemodiálisis.
Estos procedimientos son realizados por personal nefrológico especializado en la unidad de terapia intensiva con un circuito que se arma y diseña en un área adecuada y limpia. Una de las principales ventajas que se le adjudican a estas terapias es la tolerancia hemodinámica a la extracción de grandes volúmenes de líquido en forma gradual y controlada, en pacientes en estado crítico.
Principios
- La convección es un movimiento del agua a través de una membrana semipermeable como resultado del gradiente de presión hidrostática transmembrana.No requiere solución dializante. El agua difunde por gradiente de concentración a través de ésta, equilibrando la concentración.
- La hemofiltración se produce por una fuerza hidrostática u osmótica a través de una membrana semipermeable (hemoconcentrador) por medio de una fuerza convectiva y por gradiente de presión, el ultrafiltrado resultante está constituido por agua plasmática, electrolitos como potasio, sodio, creatinina, urea, glucosa (sustancias cuyo peso molecular sea menor a 50,000 daltons).
- La suma del promedio de presión sanguínea positiva y el valor absoluto de la presión negativa filtrada es la presión hidrostática de la membrana.
- La presión transmembrana es un regulador de la velocidad de ultrafiltrado.
- Las membranas biocompatibles promueven la activación del complemento y los granulocitos al entrar en contacto con la sangre del paciente.
Ventajas
- Evita cambios bruscos de volemia, ofrece mayor estabilidad hemodinámica.
- Mejor control metabólico y hemodinámico a la extracción de grandes volúmenes de líquido.
- Se eliminan pequeñas y medianas moléculas por lo tanto hay remoción de mediadores de respuesta inmune activados en el choque séptico, y responsables de la respuesta inflamatoria sistémica y el fallo multiorgánico.
- Permite gran flexibilidad electrolítica, hay un bajo volumen sanguíneo extracorpóreo (100 mL aproximadamente) por lo que hay menor activación del complemento.
- En pacientes con insuficiencia cardíaca descompensada, la disminución del gasto cardíaco activa mecanismos neurohumorales de retención hidrosalina, pudiendo ocasionar incluso, insuficiencia renal. El fallo ventricular sostenido hace que el paciente se sobrehidrate, empeorando el cuadro y manteniendo un círculo vicioso. La HFVVC, permite la extracción del volumen retenido, mejora la performance ventricular, disminuye la activación neurohumoral, y a veces restaura la diuresis.
Indicaciones
Pacientes pediátricos y adultos:- Insuficiencia renal aguda.
- Falla orgánica múltiple.
- Choque séptico.
- Insuficiencia cardíaca.
Contraindicaciones
Pacientes pediátricos y adultos:- Dificultad de acceso a la red vascular del paciente.
- Inestabilidad hemodinámica severa
- Hipotensión arterial relativa
- Existencia de sangrado activo o hemorragia cerebral reciente, si no puede prescindirse de la heparinización.
Complicaciones
Pacientes pediátricos y adultos:- Relacionadas al acceso vascular, disfunción mecánica, trombosis, hemorragia e infección, desconexión de los tubos del circuito, embolia aérea, pérdida aguda de volumen, formación de trombos en el circuito.
- Relacionadas a la punción arterial, hematoma, sangrado, neumotórax.
- Relacionadas a la velocidad de hemofiltrado, descompensación hemodinámica, alteraciones electrolíticas y arritmias
Hemofiltración
La depuración de solutos se realiza exclusivamente por el principio de convección, sin baño de diálisis, a semejanza del funcionamiento del riñón nativo. La eliminación de solutos en la hemofiltración depende del coeficiente de cribado (cociente entre la concentración del soluto en el ultrafiltrado y en el agua del plasma) y de la tasa de ultrafiltración.
Para conseguir una dosis de diálisis adecuada según los criterios basados en la eliminación de urea, es necesario conseguir en cada enfermo un volumen de ultrafiltración equivalente a su volumen de distribución de la urea (un mínimo de 30 l). Para obtener una tasa tan alta de ultrafiltración es necesario un flujo de sangre superior a 400 ml/min. Este requisito y el elevado volumen requerido de líquido de reposición hicieron que esta técnica, tan antigua como la hemodiálisis, tuviera un escaso desarrollo.
Hemodiafiltración
La hemodiafiltración combina los dos principios de difusión y convección. Con flujos arteriales menores y tasas de ultrafiltración de hasta 12 litros por sesión, se consigue un aclaramiento de pequeñas moléculas muy superior al de la hemofiltración, con una eliminación de moléculas medianas y grandes intermedia entre la hemodiálisis y la hemofiltración.
Hay que resaltar que difusión y convección no tienen un efecto aditivo, sino que se interfieren mutuamente en la transferencia de moléculas. La eliminación difusiva de un soluto disminuye su concentración plasmática conforme progresa la sangre por el dializador y reduce su eliminación convectiva, que es proporcional a su concentración en el compartimento sanguíneo. Por otra parte, la eliminación convectiva aumenta la concentración del soluto en el compartimento del baño de diálisis, con disminución del gradiente de concentración transmembrana y de la eliminación difusiva.
Además de la hemodiafiltración estándar, hay otras dos modalidades que utilizan los principios de la hemodiafiltración: la biofiltración sin acetato (AFB) y la paired filtration dialysis (PFD).
Biofiltración sin acetato (AFB)
Es una técnica de hemodiafiltración en la que el líquido de diálisis no contiene ninguna base (ni acetato ni bicarbonato). La tasa de ultrafiltración extra es de 6-10 litros y el líquido de reposición es una solución de bicarbonato sódico. El objetivo de esta técnica es eliminar el acetato del baño de diálisis y controlar el equilibrio ácido-base de una forma individualizada. Para garantizar un correcto ajuste, es preciso efectuar controles de las concentraciones de bicarbonato en sangre pre diálisis y pos diálisis al inicio de la técnica y siempre que se modifiquen las condiciones de la diálisis (tiempo, flujo arterial, superficie.
Dialisis Y Filtracion Emparejadas - Paired Filtration Dialysis (Pfd)
Es una técnica de hemodiafiltración diseñada para evitar la interferencia entre los transportes convectivo y difusivo. Consta de dos dializadores acoplados en serie. En el primero se realiza una ultrafiltración de 9-12 litros y en el segundo una hemodiálisis tradicional; en la conexión existente entre ambos se efectúa la reinfusión del líquido de reposición.
La PFD con regeneración del ultrafiltrado es una modalidad derivada de la anterior. El líquido ultrafiltrado en la primera cámara es reinfundido tras ser regenerado en un cartucho que adsorbe toxinas urémicas. Esto evita la necesidad de líquido de sustitución y aumenta la seguridad de la técnica, ya que el volumen ultrafiltrado es el mismo que es reinfundido, sin posibilidad de desequilibrio entre ultrafiltración y reinfusión.
Convección online
La posibilidad de usar el baño de diálisis como líquido de sustitución fue la idea que renovó el interés por las técnicas convectivas. Inicialmente, se utilizó como líquido de reposición un baño de diálisis que previamente había sido esterilizado y almacenado en recipientes cerrados (preparación offline del líquido de reposición). Pero fue la infusión directa en la sangre del baño de diálisis conforme se va produciendo en el monitor, sin necesidad de almacenamiento externo (preparación online), el gran avance técnico que permitió la expansión de las técnicas convectivas en el tratamiento de la insuficiencia renal crónica.
Para poder usarlo como líquido de reposición, el baño de diálisis debe ser de alta calidad y reunir las condiciones del denominado baño ultrapuro. Tiene que ser fabricado con agua de gran pureza obtenida con doble sistema de ósmosis inversa, debe estar en continua recirculación para evitar focos de contaminación por estancamiento, y antes de ser infundido en el circuito sanguíneo debe atravesar al menos dos filtros de endotoxinas intercalados en el circuito del agua y del baño de diálisis.
Esta técnica de producción online permite utilizar grandes volúmenes de reposición sin incremento del coste. Se supera así una de las principales limitaciones de la convección clásica, y se consigue un alto rendimiento en la eliminación de sustancias por convección. Un módulo de balance de fluidos o un sistema similar con medidores de flujo garantiza una exacta equivalencia en el tiempo entre el exceso de volumen plasmático extraído y el volumen repuesto.
Aunque la convección online se ha aplicado a las técnicas de hemofiltración, PFD y hemodiafiltración, es esta última la que ha logrado un mayor desarrollo, y en la actualidad es la técnica convectiva online por antonomasia.
Hemodiafiltración online
No se utiliza en Estados Unidos, pero es una técnica en expansión creciente en Europa y Asia. La hemodiafiltración online con infusión del líquido de sustitución en modo posdilucional es el procedimiento que consigue los mejores resultados en la depuración de todo tipo de moléculas. El volumen de recambio ha ido aumentado con los avances tecnológicos. La Guía Clínica del año 2006 para Unidades de Diálisis de la Sociedad Española de Nefrología establece un volumen mínimo de 15 litros y recomienda, si fuera posible, que sea superior a 20 litros (hemodiafiltración posdilucional de alto volumen).
Este volumen de recambio no siempre puede conseguirse. Como se describió previamente, una fracción de filtración mayor del 30% puede ocasionar problemas de rendimiento del dializador, con aumento de la presión transmembrana y aparición de alarmas. Para conseguir un volumen adecuado de recambio, el flujo de sangre debe ser superior a 350 ml/min.
La libre disposición de líquido de reposición ha permitido el desarrollo de otros modos de hemodiafiltración online para su uso en enfermos con hematocrito alto y en los que el flujo arterial no pueda alcanzar las altas tasas requeridas. La infusión del líquido de reposición antes de entrar la sangre en el dializador (modo predilucional) disminuye los problemas derivados de la hemoconcentración y polarización. El descenso de la concentración de solutos en el agua del plasma como consecuencia de la hemodilución reduce su transferencia por difusión y por convección. Aunque se intenta compensar esta pérdida de eficacia aumentando el volumen de recambio (como mínimo debe ser el doble que en el modo posdilucional), el rendimiento del modo predilucional siempre es inferior.
Para mejorar la eficacia del modo predilucional y evitar los problemas derivados del aumento de la presión transmembrana en el posdilucional, han surgido diversas modalidades de hemodiafiltración online. Las más conocidas son:
- Modalidad mixta simultánea: el líquido de reposición es infundido predializador y posdializador de forma simultánea.
- Modalidad secuencial: se inicia en modo posdilución y se pasa al predilución cuando la presión transmembrana alcanza un determinado valor.
- Modalidad mid-dilution: utiliza un dializador especial con dos haces de capilares (central y anillo periférico); la sangre circula sucesivamente por ambos haces en recorrido de ida y vuelta, y entre ambos se realiza la infusión del líquido de reposición; la primera parte del recorrido se comporta como una hemodiafiltración en modo posdilucional y la segunda como una hemodiafiltración en modo predilucional.
- Modalidad posdilucional automatizada: la tasa de ultrafiltración se autorregula en función del flujo de sangre y de la presión transmembrana.
Todas estas modalidades consiguen unos resultados intermedios entre la predilucional y la posdilucional.
Nefrología Digital – Sociedad Española de Nefrología 2011
Fundacion Alcer - 2013
http://alcer.org/fundacionalcer/wp-content/uploads/2013/11/moreso1.pdf
Nephrology Dialysis and Transplantation – Oxford Journals 2012
DR. FERNANDO VASQUEZ MENDOZA
Trasplante Renal
El TRASPLANTE RENAL es un procedimiento quirúrgico en el cual se coloca o implanta un riñón sano en un paciente con Insuficiencia Renal Crónica Grado V o Terminal.
Después del trasplante de cornea, el trasplante renal debe ocupar el segundo lugar en el mundo. En Estados Unidos se realizan aproximadamente 15,000 trasplantes de riñón al año. En Europa
El trasplante renal tiene en sí una mortalidad muy pequeña, la medicación inmunosupresora supone sin duda alguna un riesgo adicional pero tampoco muy grande, y el paciente se ve libre de la terapia de diálisis crónica.
Por otra parte, y al menos por hoy, los órganos disponibles para trasplantar son un bien escaso, su número es claramente inferior al necesario; las listas de espera para trasplante aumentan año tras año, y hay pacientes que no llegan nunca a ver realizado su SUEÑO DE RECIBIR EL ÓRGANO SALVADOR.
Historia Mundial
La Historia del Trasplante se remota a hace 3,000 años. La sustitución de órganos inservibles por otros nuevos ya aparecía en la Mitología. Dioses quiméricos aparecen en todas las culturas. Así se inicia la etapa llamada Protohistoria del Trasplante (Dr. Carretero – Barcelona).
Las técnicas de anastomosis vasculares se perfeccionaron entre 1896 y 1902, logrando las bases para el éxito posterior de los trasplantes de órganos (Von Exner, Ullman, Carrel). ALEXIS CARREL RECIBE EL PREMIO NÓBEL DE FISIOLOGÍA Y MEDICINA EN 1912.
Posteriormente entre 1903 y 1950, se continuaron y lograron éxito una serie de trasplantes experimentales en animales (Ungen, Florezco, Villar, Williamson, Avramovici, Ibuja, Parkinson, etc).
Sin embargo, simultáneamente muchos intentos se realizaron en humanos (Voronoy, Landsteiner, Hume, Lawler, Kuss, Hamburger, etc.)
Los primeros trasplantes de riñón exitosos fueron hechos en Boston ( Hume, Merril, Millar y Thorn) y París (Michon, Hamburger y Richet) entre 1951 y 1954. El 23 de Diciembre de 1954 en Bostos, Murray, Merril y su equipo realizan el primer trasplante entre los gemelos idénticos (Ronald y Richard Herrick), para eliminar cualquier problema de una reacción inmune. La popularización del trasplante renal fue lenta.
Entre 1954 y 1959 se realizaron aproximadamente 30 isotrasplantes (EEUU, Reino Unido, Francia, Canadá).
El trasplante de donante cadavérico se introdujo en 1964, cuando comenzó el uso rutinario de medicamentos para prevenir y tratar el rechazo agudo.
Para evitar el rechazo se empezó utilizando la radiación subletal de la medula (Merril, Murria, Kuss), luego azatriopina (Schwartz), corticoides (Goodwin) y posteriormente con la Ciclosporina (1977), se apertura una serie de investigaciones hacia nuevos medicamentos inmunosupresores Micofenolato, Tracolimus, Rapamicina, Sirulimus,etc.
El Riñón era el órgano más fácil a trasplantar, pues la prueba de compatibilidad de tejidos era simple, el órgano era relativamente fácil de extirpar e implantar, los donantes vivos podían ser usados sin dificultad, y en caso de fallo, la diálisis renal estaba disponible desde los años 1940. La prueba de compatibilidad de tejidos es esencial para el éxito.
Gracias a su invalorable contribución a la Medicina, el Dr. JOSEPH EDWARD MURRAY, RECIBIÓ EL PREMIO NOBEL DE MEDICINA EN 1990.
Sistemas de Histocompatibilidad
El desarrollo del Trasplante de Órganos va ligado a un mejor conocimiento de la Inmunológica. La puesta en contacto con células extrañas a un organismo con el sistema inmunológico de éste, pone en marcha un mecanismo encargado de la identificación y destrucción de estas células.
Las pruebas de Histocompatibilidad evalúan estos sistemas:
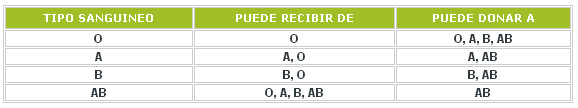
Compatilidad Sistema ABO
Compatilidad Sistema HLA
- Clase I: Locus A, B, C
- Clase II: Locus DR, DP, DQ
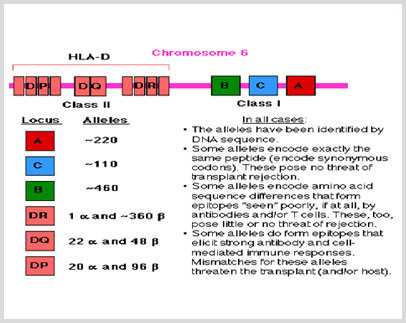
Crossmacht o Prueba Cruzada:
Entre el suero del receptor y células linfoides del donante, que pondrán evidencia de anticuerpos circulantes contra antígenos del donante.
El donante y el receptor tienen que ser de grupo sanguíneo ABO compatible (ver tabla) e idealmente deben compartir tantos HLA como sea posible, finalmente el crossmatch debe ser compatible (negativo). Esto disminuye el riesgo de rechazo, la necesidad de diálisis, y de un futuro trasplante. En los Estados Unidos, hasta un 17% de todos los trasplantes riñón de donantes fallecidos tienen HLA que concuerdan.
El Receptor
Evaluación pre Trasplante Renal- Evaluación Clínica General.
- Panel de Anticuerpos.
- Exámenes Bioquímicas: Perfil hematológico, renal, hepático, de coagulación, lipidico.
- Imágenes: Ecografía abdominal.
- Serología Viral completa.
- Coproparasitologico, Urocultivo.
- Endoscopia Tracto gastrointestinal
- Evaluación Urológica: Cistoscopia, PSA
- Evaluación Cardiológica: EKG, Eco cardiografía, Rx de Tórax.
- Descarte de focos infecciosos: Odontología, Otorrinolaringología.
- Mamografía, PAP de cervix (en mujeres)
Contraindicaciones para ser considerado Apto para un Trasplante Renal
- Enfermedad Cardiovascular severa
- Enfermedad Pulmonar severa
- Enfermedad Hepática severa
- Infección Terminal incurable: SIDA
- Cáncer activo
- Evidencia clara de no-aceptación previa de medicación alguna (Non compliance)
- Enfermedad Mental severa.
La Lista de Espera
Para seleccionar el receptor se dispone de una lista donde están los nombres y los datos necesarios que permitan decidir, ante un órgano concreto disponible, el receptor más adecuado.Considera varios factores a saber:
- Clave: Historia, Análisis, Complicaciones actuales y anteriores.
- Teléfonos
- Dirección - Ciudad
- Edad
- Tiempo en Diálisis: Fecha de Ingreso a programa de Diálisis Crónica
- Grupo Sanguíneo
- HLA Clase I
- HLA Clase II
- Panel de Anticuerpos: Resultados Históricos
La responsabilidad de seleccionar al mejor receptor cuando existe un donante cadavérico potencial recae en una Organización dependiente del Ministerio de Salud, la cual idealmente debe congregar a los representantes más idóneos de todos los sistemas de salud involucrados en los trasplantes, léase Ministerio de Salud, Seguridad Social, Privados y Fuerzas Armadas.
En un sistema de Salud Universal, el receptor puede depender de cualquiera de los sistemas de salud mencionados, realizándose así el trasplante en cualquier centro trasplantador.
El Donante Renal
ClasificaciónEl donante renal debe ser:
- Donante Vivo Familiar
Un DONANTE VIVO FAMILIAR, genéticamente emparentado con el receptor, como uno de los padres, un hermano o los hijos - Donante Vivo No Familiar
Un DONANTE NO EMPARENTADO con el receptor, como un amigo o el cónyuge. - Donante Cadavérico
Un Donante en Muerte Cerebral: Aun con corazón latiendo y perfundiendo órganos.
Donante en Parada Cardiaca: Con corazón no latiendo. Debe recibir anticoagulacion, el tiempo es mucho más corto para la utilización de los órganos.
En el caso de Donante Vivo, la operación es programada, el tiempo de espera se reduce al tiempo de evaluación del donante, el donante debe dar previamente su consentimiento informado, el tiempo de recuperación es aproximadamente de 4 a 6 semanas.
Procedimiento de la Donación de Órganos
DONAR: Dar esperanza a un ser humano sin esperanza…la esperanza de vivir.
Confirmar que el paciente donante vivo o cadavérico reúna las condiciones clínicas adecuadas:
En el Donante Vivo:- Donación Voluntaria, libre de coerción
- Persona adulta, racional y consciente de sus decisiones.
- Evaluación Clínica General
- Serología Viral completa
- Perfil hematológico, hepático, renal, lipidico, de coagulación.
- Imagenología: Ecografía abdominal, Radiografía de tórax, Urografía excretoria, TEM de arterias renales.
- Evaluación Psicológica.
- Autorización del paciente en vida (Documento de Identidad) o de los familiares (Legal)
- Serologia Viral Completa
- Perfil bioquímico, hematológico, renal, hepático, de coagulación.
- Imagenologia: Ecografía abdominal.
Procedimiento Quirúrgico
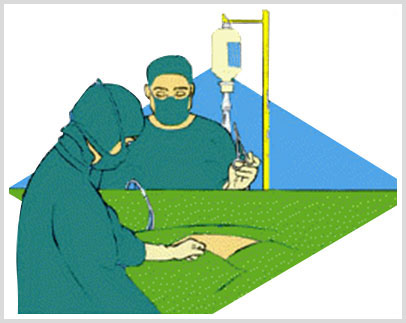
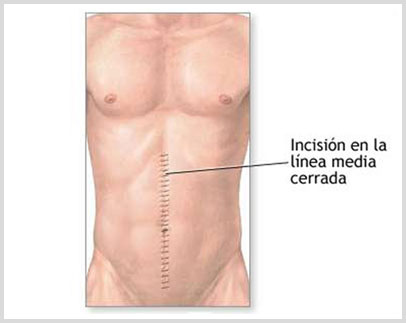
Con el paciente previamente sometido a anestesia general, según sea la indicación del Jefe del equipo de Trasplante, se procede a realizar una incisión mediana abdominal, se procede luego de ubicar los vasos sanguíneos y el uréter del riñón, a su clampaje y extracción del órgano, para luego hacer hemostasia y proceder a cerrar el abdomen en la zona de la incisión. Actualmente se utilizan incisiones pequeñas para la nefrectomía a través de técnicas de Laparoscopia (mano asistida).
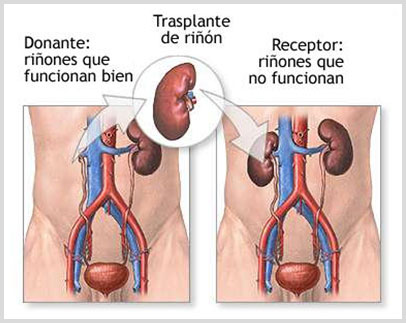
Aunque los donantes en MUERTE CEREBRAL (o con 'corazón latiendo') son considerados que están muertos, el corazón del donante continúa bombeando y manteniendo la circulación. Esto permite que los cirujanos comiencen a operar mientras los órganos todavía están siendo perfundidos. Durante la operación, la aorta será canulada, y después la sangre de los pacientes será sustituida por una solución helada de almacenamiento, como UW (Viaspan), HTK o Perfadex (más de una solución puede ser usada simultáneamente dependiendo de cuáles son los órganos a trasplantar). Debido a la temperatura de la solución, una vez que se vierten grandes cantidades de solución de cloruro de sodio frío sobre los órganos (para un rápido enfriamiento éstos) el corazón deja de bombear.
Los donantes cadavéricos en PARADA CARDIACA son aquellos a los que no les late el corazón son pacientes que no entran dentro del criterio de muerte cerebral, pero no tienen ninguna oportunidad de recuperación. En este procedimiento, el tratamiento es por abstención (se apaga la ventilación mecánica).
Normalmente, algunos minutos después de que la muerte se haya producido, rápidamente, el paciente es llevado al quirófano, donde los órganos son extraídos, después de lo cual la solución de almacenamiento es irrigada a través de los órganos directamente. Dado que la sangre ya no está circulando, la coagulación debe prevenirse con grandes cantidades de agentes anticoagulantes, como la heparina.
Luego el riñón saludable se transporta en una solución preservante especial refrigerada que preserva el órgano hasta por 48 horas, el mecanismo de transporte puede ser en un recipiente convencional o en equipos médicos especializados.
Esto permite brindar tiempo adicional para que se hagan las pruebas necesarias para determinar la compatibilidad de la sangre y el tejido del donante y el receptor. Dichas pruebas se llevan a cabo antes de la operación; este periodo de tiempo permite además que todo el personal del centro trasplantador logre estar en el momento adecuado para la cirugía de Trasplante Renal.
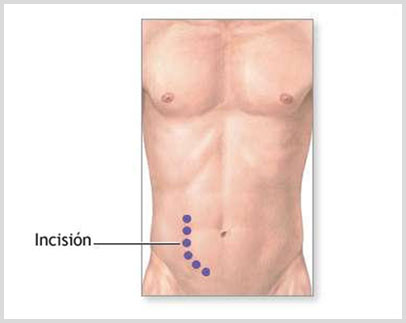
Mientras el paciente se encuentra profundamente dormido y sin dolor, bajo anestesia general se realiza una incisión en la parte inferior del abdomen, luego de ubicar los vasos arteriales y venosos adecuados se procede a colocar el nuevo riñón debajo del abdomen inferior (izquierdo o derecho) y conecta la arteria y la vena del riñón nuevo con la arteria y vena (iliaca externa o hipogástrica) del paciente. Luego de confirmar que las anastomosis están bien, se procede a desclampar los vasos sanguíneos, con lo cual la sangre del paciente fluye hacia el nuevo riñón, el cual inicia su trabajo de filtración y excreción, presentado buen flujo urinario en la sala de operaciones.
Luego se procede a la anastomosis de uréter del riñón nuevo con la vejiga del paciente, realizando una tunelizacion del uréter en la pared vesical (Técnica de Lich Gregorie). Finalmente se procede a realizar Hemostasia, no sin antes verificar nuevamente la patencia de los flujos sanguíneos, y las características adecuadas del injerto; luego se procede a cerrar el abdomen por planos y finalmente la incisión.
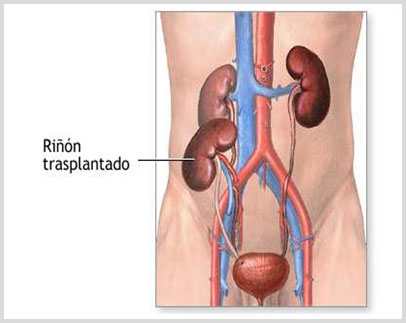
Evolución Post Operatoria en la Clínica
En el caso del Paciente Trasplantado (RECEPTOR) el periodo de recuperación y observación es en promedio de 7 a 10 días, después de ello, el paciente requiere un seguimiento estricto y un control semanal de con exámenes de laboratorio y la evaluación ecografía doppler del injerto.
En el caso del DONANTE VIVO, el periodo de recuperación es de 4 a 6 días. Las suturas se retiran aproximadamente a la semana. De 4 a 6 semanas el paciente debe evitar mayor actividad.
Riesgos del Trasplante Renal
Los riesgos que implica el Trasplante Renal están relacionados a la Anestesia, a la Cirugía en sí, a los medicamentos inmunosupresores, a las infecciones propias de un pacientes inmunocomprometido.
- Los riesgos inherentes a la Anestesia son: - Reacciones adversas a los Anestésicos
- Los riesgos secundarios a la Cirugía de Trasplante: - Sangrado
- Los riesgos adicionales como paciente trasplantado: - Rechazo del Órgano
- Problemas Respiratorios
- Infección de Herida operatoria
- Linfocele
- Trombosis de Injerto
- Infección oportunistica o no oportunistica
- Eventos adversos a la medicación Inmunosupresora
- Hipertensión Arterial
- Diabetes Mellitus
- Dislipidemia
- Cáncer
Evolución Clínica y Pronóstico
El trasplante renal es el tratamiento que ofrece el mejor pronostico para los pacientes con Insuficiencia renal Crónica en grado V (Terminal). La mayoría de los centros trasplantadores tienen una tasa de sobrevida de pacientes superior al 90 % al primer año, y de mas del 80 % a los 3 años.
A los 15 años, la tasa de órganos renales funcionales se encuentra alrededor del 50 %.
Es cierto también que los órganos provenientes de donantes vivos funcionan mejor que los de donantes cadavéricos.
Todo paciente trasplantado debe continuar un tratamiento de por vida con medicamentos Inmunosupresores, con el fin de evitar la aparición del Rechazo del Injerto Renal, el cual responde al sistema Inmunológico del paciente identificando el riñón trasplantado como extraño y procediendo a destruirlo.
Este tratamiento crónico, tiene un riesgo adicional ya mencionado en líneas arriba, la presencia de Infecciones y de Cáncer. El riesgo de Infecciones oportunisticas es mayor en los primeros 6 meses del trasplante, motivo por el cual el paciente debe estar bajo un régimen de medicación profiláctica. Con relación al riesgo de cáncer, el paciente deberá tener anualmente una evaluación integra de screeening de Cáncer.
Los años de vida ganados son más para pacientes más jóvenes, pero incluso los pacientes de 75 años, el grupo de edad más avanzada para el que hay datos, gana un promedio de 4 años de vida con un trasplante de riñón.
El éxito del trasplante renal dependerá del seguimiento clínico estricto y el cumplimiento minucioso del esquema de tratamiento inmunosupresor y complementario.
Reflexiones Finales
Es un hecho demostrado y contrastado que los pacientes portadores de un trasplante renal disfrutan de una buena calidad de vida relacionada con la salud, mejor que la de los pacientes en tratamiento crónico de Diálisis. Más aun, muchos investigadores han comprobado que la calidad de vida relacionada a la salud de las personas trasplantadas es similar a la población general.
El éxito del trasplante renal es la consecuencia de un esfuerzo coordinado de todo el equipo medico de salud que incluye el nefrólogo, el cirujano de trasplante, el coordinador de trasplante, el farmacéutico, el nutricionista y el Trabajador social. Sin embargo los miembros más importantes del equipo de salud son TÚ Y TU FAMILIA, estoy convencido que no existe un mejor paciente y los mejores respectivos familiares quienes estén bien y adecuadamente informados de todo lo concerniente al trasplante renal, la evaluación clínica previa, los riesgos, las complicaciones a corto y largo plazo, medidas de prevención de dichas complicaciones, alimentación, controles clínicos y de laboratorio posteriores al trasplante, etc.
“Todo progreso es continuo, una generación lo inicia, otra lo germina, la siguiente lo ve florecer y finalmente surge el fruto que puede extenderse a todo el mundo “(Murray, 1982)
Dr. Fernando Vásquez – Dr. Primo Pacheco
Clínica San Felipe - 1994
DR. FERNANDO VASQUEZ MENDOZA

|

